Introducción
La enfermedad de Kawasaki (EK), también conocida como síndrome mucocutáneo linfonodular, es una vasculitis aguda autolimitada de etiología desconocida con rasgos clínicos característicos descritos por primera vez en niños japoneses en 19671. Estos rasgos clínicos siguen siendo el pilar del diagnóstico de la EK e incluyen fiebre, conjuntivitis bilateral no purulenta, erupción cutánea, linfadenopatía cervical y cambios mucocutáneos2. Sin embargo, el diagnóstico puede ser difícil, ya que las características clínicas se solapan con muchas enfermedades febriles pediátricas comunes y el amplio espectro de presentaciones clínicas incluye tanto características clínicas incompletas como presentaciones atípicas. Sin embargo, el diagnóstico y el tratamiento rápidos son esenciales para reducir la importante morbilidad cardíaca asociada a la EK3.
Es una enfermedad que suele aparecer en niños pequeños, estando por debajo de los 5 años el 80% de los pacientes afectados, pero puede presentarse a cualquier edad, incluso en adultos4. Aunque esta enfermedad se ha descrito en todo el mundo, el mayor número de casos se ha notificado en los países del noreste de Asia, como Japón, Corea y Taiwán5. En España se desconoce la incidencia general, pero se describió una incidencia en Cataluña de 8/100.000 niños menores de 5 años entre 2004-20136.
La complicación más grave de la EK son los aneurismas de las arterias coronarias (AAC). La EK es la causa más común de cardiopatía adquirida entre los niños de los países desarrollados7 y un factor de riesgo de infarto de miocardio en la edad adulta temprana8. En un metaanálisis reciente se identificaron cuatro factores de riesgo para desarrollar AAC: el sexo masculino, la resistencia a la inmunoglobulina intravenosa (IgIV), el tratamiento con IgIV posterior a 10 días del inicio de los síntomas y el aumento de los niveles de proteína C reactiva9. De hecho, se ha observado que el tratamiento temprano con IgIV y con terapia adicional de corticosteroides reduce el riesgo de AAC hasta el 58%10.
Disponer de protocolos clínicos sustentados en una sólida base científica y consensuados por los especialistas implicados constituye una valiosa herramienta que aporta información a los profesionales y ayuda en el proceso de toma de decisiones.
El consenso es crucial para desarrollar un protocolo. La técnica Delphi se erige como un método de consenso para abordar un tema complejo, mediante un panel de expertos a través de cuestionarios iterativos en las que las respuestas de una encuesta se resumen y comparten posteriormente para la consideración del grupo11. Además, en los últimos años tanto a nivel internacional como en nuestro contexto, la participación de pacientes surge como un imperativo para incorporar la perspectiva, experiencias e intereses de los pacientes12.
El objetivo de este trabajo fue elaborar un protocolo asistencial, para el diagnóstico y abordaje de la enfermedad de Kawasaki, basado en la evidencia disponible de literatura sobre recomendaciones.
Material y método
Se realizaron una revisión sistemática y una encuesta a pacientes y familiares, y con sus resultados se elaboraron una serie de recomendaciones para evaluar por un panel de expertos mediante metodología Delphi.
2.1 Revisión sistemática
Se realizó una revisión sistemática mediante la búsqueda de las recomendaciones en guías de práctica clínica, informes de evaluación de tecnologías sanitarias, revisiones sistemáticas, metaanálisis, documentos de consenso, posicionamientos y protocolos de Sociedades Científicas a través de una búsqueda bibliográfica en las bases de referencias MEDLINE (mediante OVID), EMBASE, Web of Science (WOS), Epistemonikos database y Cochrane Library con los términos “'mucocutaneous lymph node síndrome”, “Kawasaki disease” y “Kawasaki syndrome”. También se buscó en páginas web específicas de guías de práctica clínica. Estas búsquedas se realizaron hasta febrero de 2020 (Anexo 1, material suplementario).



Se leyeron a texto completo los documentos seleccionados por dos autores (SBL y JMML) y, en caso de discrepancias se resolvieron mediante discusión y consenso. Se extrajeron de su contenido las recomendaciones que incluían los documentos, elaborando con ellas una lista, integrando las redundantes que no aportaran matices diferentes.
Las GPC identificadas que cumplían los criterios de selección preestablecidos se evaluaron mediante el instrumento AGREE II con el objetivo de evaluar su calidad13. El análisis se realizó de forma independiente por 2 evaluadores (LAC y JMML), que valoraron cada uno de los elementos que componen los seis dominios del instrumento. Se decidió seleccionar como guías base a aquellas que superasen al menos la puntuación de 3 sobre 7 en la calidad global de la guía. Además, las guías debían presentar un nivel de evidencia y grado de recomendación asociado a cada juicio. La lectura crítica de las revisiones sistemáticas se realizó independientemente por parte de 2 investigadores (LAC y JMML), utilizando la herramienta AMSTAR II14. Las discrepancias fueron resueltas mediante discusión y consenso.
Se siguieron las recomendaciones de Humphrey-Murto, et al.15 para valorar la calidad metodológica de los estudios que emplearan un método de consenso.
2.2 Encuesta a pacientes
Con el objetivo de incorporar la perspectiva, experiencia e intereses de las personas con EK y sus cuidadores, en el diseño y desarrollo de este protocolo, se contó con la participación de representantes de la asociación de pacientes Asenkawa (Asociación Enfermedad de Kawasaki). Se realizó una consulta a personas de esta asociación a través de un cuestionario telemático mediante un muestreo intencional. Los participantes fueron pacientes y familiares, de diferentes regiones del territorio nacional, con diagnóstico de EK (Anexo 2, material suplementario).







2.3 Consenso de expertos mediante metodología Delphi
Como método de consenso usamos la técnica Delphi para abordar el diagnóstico y manejo de la enfermedad de Kawasaki. Tanto el número de profesionales involucrados, el problema abordado, el anonimato de las respuestas de los participantes como el tiempo disponible para realizar nuestro estudio, fueron adecuados para su desarrollo.
Se contactó con nueve profesionales implicados en la atención a la EK desde distintos ámbitos asistenciales: Pediatría de Atención Primaria, Pediatría Hospitalaria, Medicina de Familia, Cardiología, Cardiología Pediátrica, Inmunología, Reumatología e Infectología Pediátrica. Este abordaje multidisciplinar permite cubrir los distintos puntos de acceso de atención a los pacientes con signos posibles de la enfermedad. La selección de expertos se basó en la experiencia con el diagnóstico, tratamiento o seguimiento de pacientes con EK (Anexo 3, material suplementario).

Los participantes recibieron, junto a una carta de presentación, un primer cuestionario telemático, el texto explicativo del proyecto y documentación de apoyo basada en la revisión sistemática realizada. Además, los participantes firmaron un documento en el que se hacían explícitas las relaciones que pudieran ser origen potencial de conflictos de intereses (Anexo 4, material suplementario). El cuestionario se diseñó sintetizando las recomendaciones provenientes de la literatura y extraídas de 7 GPC2,4,16-21 (una de ellas dividida en dos publicaciones17,18), 4 consensos22-25 y 18 revisiones sistemáticas26-43. Además, se incorporó información procedente de las respuestas formuladas a los pacientes o familiares. Las preguntas se formularon para ser contestadas mediante una escala Likert de importancia del 1 al 5 (1 = totalmente en desacuerdo, 2 = en desacuerdo, 3 = neutral, 4 = de acuerdo y 5 = totalmente de acuerdo). El panelista debía anotar su puntuación para cada recomendación. Se les concedió un plazo de 10-15 días para su devolución.

El equipo de investigación sintetizó las recomendaciones en base al diagnóstico, tratamiento y monitorización en fase aguda, y en el seguimiento a largo plazo y asesoramiento de los pacientes con enfermedad de Kawasaki. La encuesta fue pilotada previamente para comprobar su claridad y comprensión por 2 clínicos ajenos al estudio.
Se consideró consenso en la aceptación de la recomendación, si las votaciones de los panelistas alcanzaban una mediana de 4 o más puntos y un rango intercuartílico relativo (RIR) menor o igual a 0,40. El RIR evalúa la proximidad de las valoraciones de los expertos, cuantos más bajos sean los valores más proximidad y por tanto mayor consenso. Por otra parte, se estableció que se alcanzaría un consenso en el rechazo de la recomendación, si la mediana de las respuestas era de 2 o menos puntos y el RIR menor o igual a 0,40. Por el contrario, aquellas recomendaciones con opiniones muy polarizadas, y por tanto con un grado de dispersión en las respuestas alto (RIR > 0,40), serían incluidas en la segunda vuelta del cuestionario.
Se estudiaron asimismo las aportaciones que los panelistas hicieron a las diferentes recomendaciones. A la vista de estos resultados, se acordó la estructura del cuestionario de la segunda ronda.
Se elaboró el cuestionario de la segunda ronda con las recomendaciones en las que no se alcanzó consenso estadístico y aquellas en las que se apreciaron que las puntuaciones de las medianas eran similares, a pesar de ser recomendaciones opuestas o ligeramente enfrentadas. Se editó un cuestionario específico para cada uno de los panelistas en el que se incluyó para cada recomendación un estimador de centralización (mediana), y la respuesta dada por ese panelista concreto en la primera ronda. También se le pedía que, a la vista de los resultados de la primera ronda, volviese a puntuar las diferentes recomendaciones. Se concedió una semana para la cumplimentación de este cuestionario.
Se incluyeron en el documento final todas aquellas recomendaciones con una puntuación ≥4 en su mediana.
En la Figura 1 se ilustra esquemáticamente los pasos seguidos en la realización de la metodología de consenso empleada.
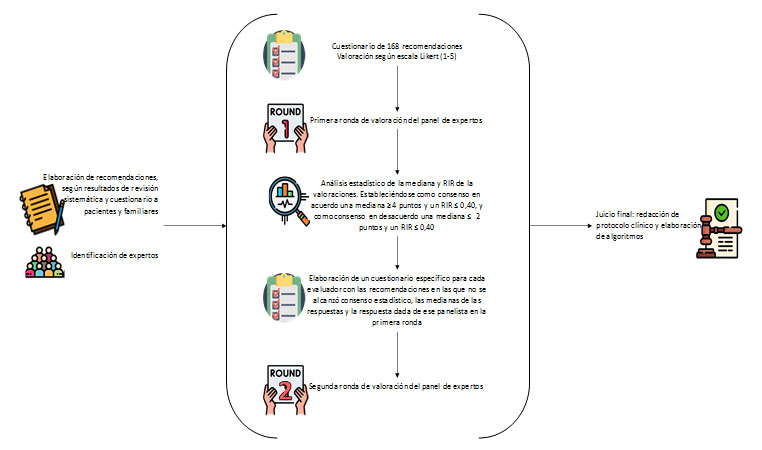
Resultados
3.1 Resultados de la revisión sistemática
Tras las dos fases de filtrado de los resultados de la búsqueda (por título y resumen, y por texto completo) según los criterios de inclusión y exclusión preestablecidos, se incluyeron un total de 30 documentos entre guías2,4,16-21, consensos22-25 y revisiones sistemáticas26-43 (Anexo 5, material suplementario). A partir de estos documentos se elaboraron los escenarios que se presentaron al panel de expertos. Los resultados de las votaciones se utilizaron para la elaboración del protocolo.
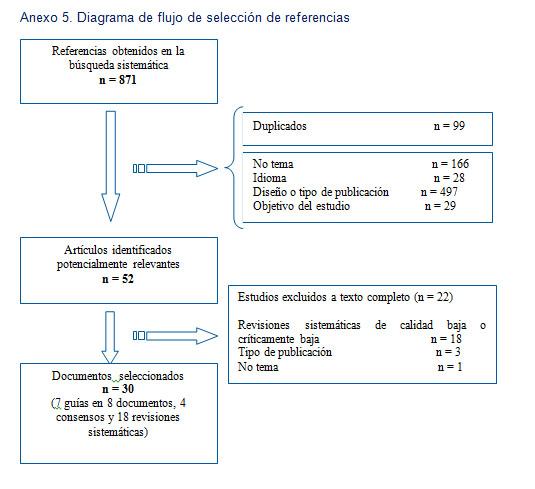
La calidad de la evidencia de las guías evaluadas fue de moderada2,4,16,19,20 a alta17,18,21. La mayoría de las revisiones sistemáticas evaluadas presentaban una calidad moderada26-36,38-43, excepto una con calidad alta37. En cuanto a los 4 consensos evaluados, 2 presentaban serias limitaciones22,23 y otros 2 cumplían la mayoría de los criterios24,25 que atestiguan su calidad.
3.2 Resultados encuesta a pacientes
Según la encuesta realizada a pacientes y familiares atendidos en distintos centros del Sistema Nacional de Salud en la que se obtuvieron 65 respuestas (93,8 % padres/madres o tutores y 6,2 % pacientes), las manifestaciones clínicas ocurrieron en todos los casos antes de los 4 años. El diagnóstico fue precoz en casi la totalidad de los casos, si bien en algún caso se demoró hasta los 3 meses. Los síntomas que aparecen entre los criterios clásicos para el diagnóstico de la EK son los más prevalentes, se referenciaron otros que aparecieron preliminarmente, pero con una frecuencia inferior al 5%, como disminución del apetito, vómitos, diarrea, cansancio-decaimiento, dolor articular y abdominal, dermatitis del pañal, artritis en las caderas, descamación escrotal, disnea, labios agrietados, rinitis o rinorrea, picor en ojos y oídos, tos e irritabilidad.
En la Tabla 1 se recogen las principales características que definen a la muestra encuestada.
Debido al tamaño muestral reducido y a la ausencia de respuestas no se pudo realizar una asociación estadística entre el seguimiento con la sintomatología presentada, por lo que no se estableció una relación con la gravedad.
3.3 Resultados de las recomendaciones Delphi
La encuesta planteada al panel de expertos contenía 168 ítems o recomendaciones divididos en 4 bloques: 1) recomendaciones diagnósticas (35 ítems); 2) recomendaciones en el tratamiento y monitorización en fase aguda de la enfermedad de Kawasaki (71 ítems); 3) recomendaciones en el seguimiento a largo plazo y asesoramiento de los pacientes con enfermedad de Kawasaki (61 ítems), y 4) recomendaciones sobre la enfermedad de Kawasaki procedentes de una encuesta a pacientes (1 ítem) (Anexo 6, material suplementario (Descargar anexo 6 PDF)).
En la primera ronda se consensuaron 150 de los 168 ítems. Aquellos sin consensuar (Bloque 1: 9 ítems; Bloque 2: 5 ítems; Bloque 3: 4 ítems y Bloque 4: 0 ítems), y 11 ítems en los que se encontraron incompatibilidades en sus enunciados y las votaciones fueron propuestos para su reconsideración en una segunda ronda.
Finalmente, se consensuaron todas las recomendaciones excepto 3 (98,2%). Una recomendación no consensuada se encontraba en el bloque de diagnóstico y 2 en el bloque de tratamiento y monitorización en la fase aguda. Se consensuaron globalmente con aceptación de la recomendación 122 ítems (72,62%), 42 ítems (25%) con consenso de la indeterminación —puntuación de la mediana >2 y <4—, 1 ítem (0,59%) con consenso en el rechazo de la recomendación y 3 ítems (1,79%) sin consenso.
Con estas recomendaciones consensuadas se llegaron a las siguientes conclusiones incluidas en el protocolo clínico y en dos algoritmos: los signos iniciales que se pueden presentar son: fiebre, cambios en las extremidades (agudos), cambios en las extremidades (subagudos), erupción, afectación conjuntival, cambios en labios y cavidad oral y adenopatías cervicales.
Se puede realizar un diagnóstico de sospecha en pacientes con presencia de fiebre, exantema e inflamación persistente En caso de presentar 4 o más signos de los anteriormente mencionados y alteraciones en las pruebas diagnósticas, estamos ante un diagnóstico de enfermedad de Kawasaki típico.
Si en las pruebas diagnósticas (pruebas de laboratorio, biomarcadores, ecocardiografía o angiografía coronaria) no se hallan las alteraciones esperadas, se recomienda el seguimiento del paciente, con una posible repetición de dichas pruebas, hasta un nuevo diagnóstico o un mayor desarrollo clínico que permita su confirmación diagnóstica. En cualquiera de los casos el estudio de los pacientes con posible diagnóstico de enfermedad de Kawasaki debe completarse con ecocardiografía coronaria, electrocardiograma y analíticas sanguínea y urinaria.
En todos los casos, se debe de comenzar el tratamiento inmediatamente tras el diagnóstico, tanto en los pacientes con la forma completa, incompleta o atípica.
Si la confirmación diagnóstica tiene lugar durante los primeros 10 días de la presentación de la sintomatología, o si el paciente presenta fiebre, indicadores inflamatorios o AAC independientemente del día del diagnóstico, el tratamiento de primera línea es IgIV 2g/kg junto con ácido acetilsalicílico (AAS) a dosis antiinflamatoria moderada (30 – 50 mg/kg/día) cada 6 – 8 horas, hasta pasadas 48 – 72 horas tras la desaparición de la fiebre.
En los casos de alto riesgo de enfermedad coronaria (pacientes menores de 12 meses o que presentan aneurismas coronarios y/o periféricos en el momento del diagnóstico) añadir metilprednisolona intravenosa (1,5 mg/kg/día) cada 12 horas durante 5 – 7 días o hasta la normalización de la proteína C reactiva. Posteriormente se pasaría a prednisona (2 mg/kg/día) con descenso progresivo durante 2 – 3 semanas.
En caso de presentar mejoría en 36-48 horas con ausencia de fiebre y un descenso de la proteína C reactiva del 50 %, se considerará que el tratamiento con IgIV ha sido efectivo y se continuará con este tratamiento junto a la administración de AAS.
En caso de no presentar mejoría en ese tiempo, se suministrará una segunda dosis de IgIV 2 g/kg, junto a metilprednisolona y AAS. Si tras ello el paciente mejora, se suprimirá la metilprednisolona, salvo en pacientes de alto riesgo que se mantendrá. Si no presenta mejoría tras esta segunda dosis, se establece que el paciente presenta resistencia a ésta, por lo que deberá ser tratado con AAS a dosis antiinflamatoria junto con metilprednisolona e infliximab. Se puede considerar la terapia con ciclosporina, anticuerpos monoclonales, agentes citotóxicos o plasmaféresis.
La medicación del paciente en la fase subaguda y convaleciente, así como su seguimiento, vendrá condicionada por su nivel de riesgo, que dependerá de la presencia o ausencia de AAC permanentes y del tamaño de los mismos en función del Z-score. Las recomendaciones en esta fase de la enfermedad se dividen en: seguimiento clínico del paciente y recomendaciones de hábitos de vida. En el caso de que el paciente presente mejoría o empeoramiento en las revisiones, el tratamiento y el seguimiento deberán ajustarse a su nueva situación.
El protocolo se representó gráficamente mediante dos algoritmos, con el objetivo de facilitar al personal sanitario la comprensión y aplicación de las recomendaciones seleccionadas y adaptadas a la práctica de nuestro entorno, sobre cómo se atenderá al paciente que presente o tenga sospecha de enfermedad de Kawasaki (Figuras 2 y 3).
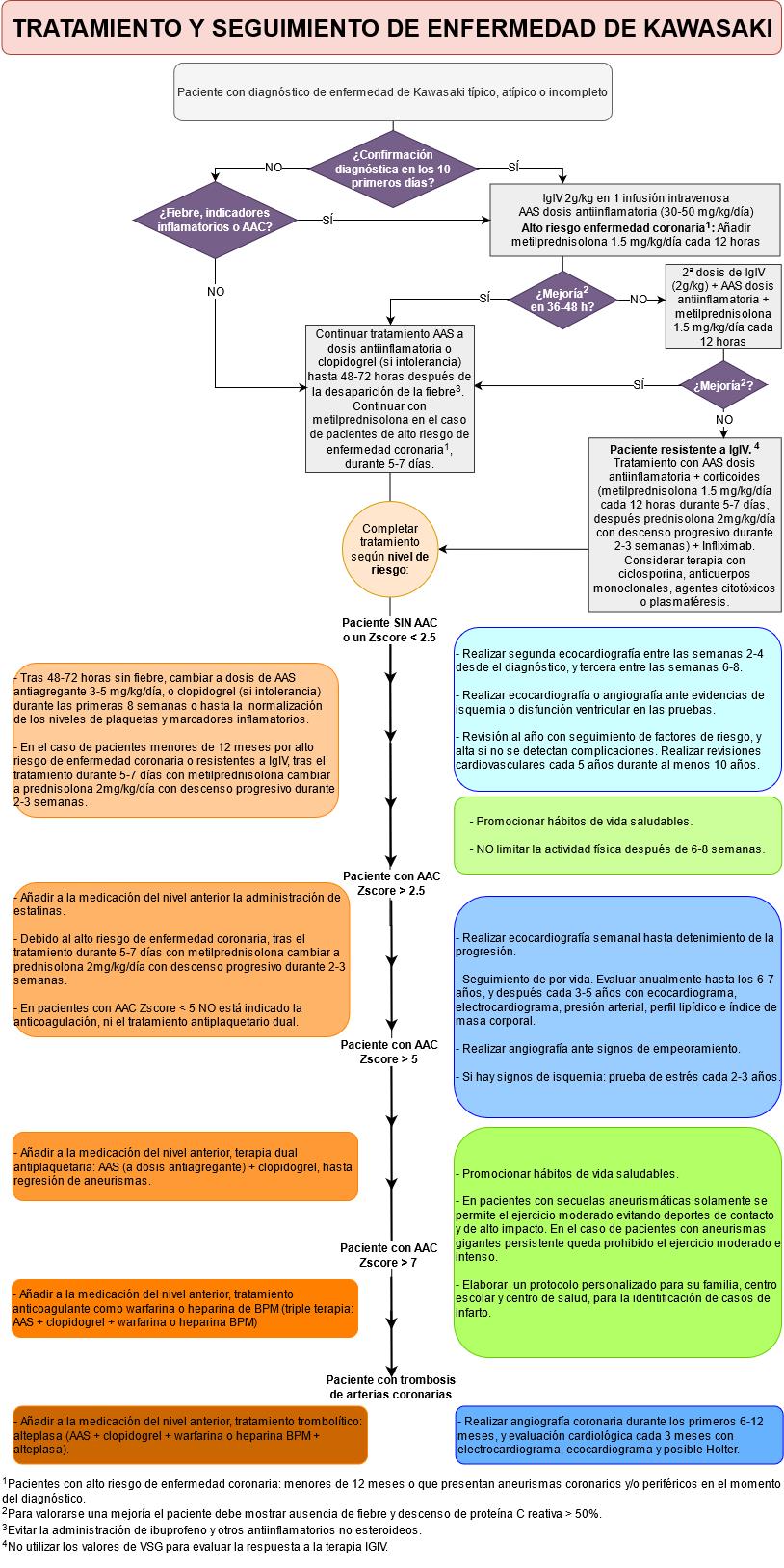
Discusión
Si bien la enfermedad de Kawasaki sigue siendo una enfermedad poco conocida, se puede controlar con un tratamiento y seguimiento adecuados. Un diagnóstico y tratamiento tempranos pueden optimizar el pronóstico y reducir las complicaciones asociadas de la enfermedad de Kawasaki. Los avances en el tratamiento y detección de la enfermedad de Kawasaki muestran un futuro prometedor. Las experiencias clínicas junto con el consenso de expertos continuarán ayudando a guiar el manejo adecuado de la enfermedad de Kawasaki.
El protocolo desarrollado y los algoritmos presentados resumen las recomendaciones procedentes de la literatura y consensuadas por un panel de expertos con diferente experiencia en el manejo y diagnóstico de la EK, para abordar un enfoque multidisciplinar desde las distintas áreas asistenciales, junto a los resultados de una encuesta a familiares o pacientes voluntarios contactados a través de la asociación Asenkawa, que aunque no ha permitido análisis estadísticos ha aportado la opinión de diversos afectados por la EK. El objetivo del protocolo es difundir las mejores prácticas en el diagnóstico, tratamiento y seguimiento de pacientes con un trastorno con múltiples aristas, de modo que se pueda prevenir la morbilidad y la posible mortalidad a largo plazo.
Un total de 26 recomendaciones para el diagnóstico y 95 para el tratamiento y seguimiento fueron aceptadas con acuerdo en la aseveración de la recomendación. No obstante, todas las decisiones clínicas deben adaptarse específicamente a cada paciente con enfermedad de Kawasaki.
Debido al constante incremento del conocimiento científico y los cambios en los sistemas de salud, las técnicas de consenso seguirán considerándose herramientas precisas para involucrar a los profesionales en la evaluación y mejora de la calidad asistencial.
Además, desde una perspectiva complementaria, los pacientes quieren ser corresponsables de su salud y, por lo tanto, han adoptado un rol diferente al tradicional, siendo necesario contar con su opinión para promover la participación y la toma de decisiones compartida. La importancia del movimiento de defensa de los pacientes aumenta de forma constante, a la vez que se incrementa su capacidad real para involucrarse en las decisiones de cobertura y financiación que podrían tener un impacto sobre sus propios tratamientos44.
Bibliografía
- Kawasaki T. Acute febrile mucocutaneous syndrome with lymphoid involvement with specific desquamation of the fingers and toes in children. Arerugi. 1967;16:178–222.
- McCrindle BW, Rowley AH, Newburger JW, Burns JC, Bolger AF, Gewitz M, et al. Diagnosis, Treatment, and Long-Term Management of Kawasaki Disease: A Scientific Statement for Health Professionals From the American Heart Association. Circulation. 2017;135:e927-e999.
- Zhu F, Ang JY. 2021 Update on the Clinical Management and Diagnosis of Kawasaki Disease. Curr Infect Dis Rep. 2021;23:3.
- JCS Joint Working Group. Guidelines for diagnosis and management of cardiovascular sequelae in Kawasaki disease (JCS 2013). Digest version. Circ J. 2014;78:2521-62.
- Singh S, Vignesh P, Burgner D. The epidemiology of Kawasaki disease: a global update. Arch Dis Child. 2015;100:1084-8.
- Sánchez-Manubens J, Antón J, Bou R, Iglesias E, Calzada-Hernandez J. Incidence, epidemiology and clinical features of Kawasaki disease in Catalonia, Spain. Clin Exp Rheumatol. 2016;34:139-44.
- Hall GC, Tulloh LE, Tulloh RM.. Kawasaki disease incidence in children and adolescents: an observational study in primary care. Br J Gen Pract. 2016;66:e271-6.
- Daniels LB, Gordon JB, Burns JC. Kawasaki disease: late cardiovascular sequelae. Curr Opin Cardiol. 2012;27:572-7.
- Yan F, Pan B, Sun H, Tian J, Li M. Risk factors of coronary artery abnormality in children with Kawasaki Disease: a systematic review and meta-analysis. Front Pediatr. 2019;7:374.
- Chen S, Dong Y, Kiuchi MG, Wang J, Li R, Ling Z, Zhou T, Wang Z, Martinek M, Pürerfellner H, Liu S, Krucoff MW. Coronary Artery Complication in Kawasaki Disease and the Importance of Early Intervention : A Systematic Review and Meta-analysis. JAMA Pediatr. 2016;170:1156-63.
- Linstone HA, Turoff M, editores. The Delphi Method. Boston: Addison-Wesley Pub; 2002.
- Toledo-Chávarri A, Perestelo-Pérez L, Álvarez-Pérez Y, Abt-Sacks A, Santoro Domingo P, Villalón D, et al. Participación de los pacientes en la Evaluación de Tecnologías Sanitarias: manual metodológico. Ministerio de Sanidad, Servicios Sociales e Igualdad. Servicio de Evaluación del Servicio Canario de la Salud; 2016.
- Brouwers M, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, et al. AGREE Next Steps Consortium. AGREE II: Advancing guideline development, reporting and evaluation in healthcare. CMAJ. 2010;182:E839-42.
- Shea BJ, Reeves BC, Wells G, Thuku M, Hamel C, Moran J, et al. AMSTAR 2: a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. BMJ. 2017;358:j4008.
- Humphrey-Murto S, Varpio L, Gonsalves C, Wood TJ. Using consensus group methods such as Delphi and Nominal Group in medical education research. Med Teach. 2017;39:14-9.
- Sociedad Argentina de Pediatría, Sociedad Argentina de Cardiología. Enfermedad de Kawasaki: Consenso interdisciplinario e intersociedades (guía práctica clínica). Versión abreviada. Arch Argent Pediatr. 2016;114:385-90.
- Marchesi A, Tarissi de Jacobis I, Rigante D, Rimini A, Malorni W, Corsello G, et al. Kawasaki disease: guidelines of the Italian Society of Pediatrics, part I - definition, epidemiology, etiopathogenesis, clinical expression and management of the acute phase. Ital J Pediatr. 2018;44:102.
- Marchesi A, Tarissi de Jacobis I, Rigante D, Rimini A, Malorni W, Corsello G, et al. Kawasaki disease: guidelines of Italian Society of Pediatrics, part II - treatment of resistant forms and cardiovascular complications, follow-up, lifestyle and prevention of cardiovascular risks. Ital J Pediatr. 2018;44:103.
- Research Committee of the Japanese Society of Pediatric Cardiology; Cardiac Surgery Committee for Development of Guidelines for Medical Treatment of Acute Kawasaki Disease. Guidelines for medical treatment of acute Kawasaki disease: report of the Research Committee of the Japanese Society of Pediatric Cardiology and Cardiac Surgery (2012 revised version). Pediatr Int. 2014;56:135-58.
- Yoon YE, Hong YJ, Kim HK, Kim JA, Na JO, Yang DH, et al. 2014 Korean guidelines for appropriate utilization of cardiovascular magnetic resonance imaging: a joint report of the Korean Society of Cardiology and the Korean Society of Radiology. Korean J Radiol. 2014;15:659-88.
- Valenzuela Flores AA (Coord). Instituto Mexicano del Seguro Social. Guía de Práctica Clínica Diagnóstico y Tratamiento de la Enfermedad de Kawasaki. (Síndrome Mucocutáneo Linfonodular). México: Instituto Mexicano Del Seguro Social; 2015.
- Barrios Tascón A, Centeno Malfaz F, Rojo Sombrero H, Fernández-Cooke E, Sánchez-Manubens J, Pérez-Lescure Picarzo J; en representación del Grupo de Cardiología Clínica SECPCC. Consenso nacional sobre diagnóstico, tratamiento y seguimiento cardiológico de la enfermedad de Kawasaki. An Pediatr (Barc). 2018;89:188.e1-188.e22.
- Brogan P, Burns JC, Cornish J, Diwakar V, Eleftheriou D, Gordon JB, et al. Lifetime cardiovascular management of patients with previous Kawasaki disease. Heart. 2020;106:411-20.
- Chowdhury D, Gurvitz M, Marelli A, Anderson J, Baker-Smith C, Diab KA, et al. Development of Quality Metrics in Ambulatory Pediatric Cardiology. J Am Coll Cardiol. 2017;69:541-55.
- de Graeff N, Groot N, Ozen S, Eleftheriou D, Avcin T, Bader-Meunier B, et al. European consensus-based recommendations for the diagnosis and treatment of Kawasaki disease-the SHARE initiative. Rheumatology (Oxford). 2019;58:672-82.
- Chen S, Dong Y, Kiuchi MG, Wang J, Li R, Ling Z, et al. Coronary Artery Complication in Kawasaki Disease and the Importance of Early Intervention: A Systematic Review and Meta-analysis. JAMA pediatrics. 2016;170:1156-63.
- Lin K-H, Chang S-S, Yu C-W, Lin S-C, Liu S-C, Chao H-Y, et al. Usefulness of natriuretic peptide for the diagnosis of Kawasaki disease: a systematic review and meta-analysis. BMJ open. 2015;5:e006703.
- Wu G, Yue P, Ma F, Zhang Y, Zheng X, Li Y. Neutrophil-to-lymphocyte ratio as a biomarker for predicting the intravenous immunoglobulin-resistant Kawasaki disease. Medicine. 2020;99:e18535.
- Yu J, Li H-H, Dong L. Meta-analysis: Diagnostic Value of N-Terminal Pro-brain Natriuretic Peptide for Kawasaki Disease. Clinical laboratory. 2016;62:1903-10.
- Cai X, Zhu Q, Wu T, Zhu B, Liu S, Liu S, et al. Association of circulating resistin and adiponectin levels with Kawasaki disease: A meta-analysis. Experimental and Therapeutic Medicine. 2020;19:1033-41.
- Dietz SM, Tacke CEA, Hutten BA, Kuijpers TW. Peripheral Endothelial (Dys)Function, Arterial Stiffness and Carotid Intima-Media Thickness in Patients after Kawasaki Disease: A Systematic Review and Meta-Analyses. PloS one. 2015;10:e0130913.
- Zhang H, Xu M-G, Xie L-J, Huang M, Shen J, Xiao T-T. Meta-analysis of risk factors associated with atherosclerosis in patients with Kawasaki disease. World journal of pediatrics: WJP. 2016;12:308-13.
- Chan H, Chi H, You H, Wang M, Zhang G, Yang H, et al. Indirect-comparison meta-analysis of treatment options for patients with refractory Kawasaki disease. BMC pediatrics. 2019;19:158.
- Crayne CB, Mitchell C, Beukelman T. Comparison of second-line therapy in IVIg-refractory Kawasaki disease: a systematic review. Pediatr Rheumatol Online J. 2019;17:77.
- Su D, Wang K, Qin S, Pang Y. Safety and efficacy of warfarin plus aspirin combination therapy for giant coronary artery aneurysm secondary to Kawasaki disease: A meta-analysis. Cardiology (Switzerland). 2014;129:55-64.
- Tanoshima R, Hashimoto R, Suzuki T, Ishiguro A, Kobayashi T. Effectiveness of antiplatelet therapy for Kawasaki disease: a systematic review. European journal of pediatrics. 2019;178:947-55.
- Wardle AJ, Connolly GM, Seager MJ, Tulloh RM. Corticosteroids for the treatment of Kawasaki disease in children. The Cochrane database of systematic reviews. 2017;1:CD011188.
- Xue L-J, Wu R, Du G-L, Xu Y, Yuan K-Y, Feng Z-C, et al. Effect and Safety of TNF Inhibitors in Immunoglobulin-Resistant Kawasaki Disease: a Meta-analysis. Clinical reviews in allergy & immunology. 2017;52:389-400.
- Yamaji N, da Silva Lopes K, Shoda T, Ishitsuka K, Kobayashi T, Ota E, et al. TNF‐α blockers for the treatment of Kawasaki disease in children. Cochrane Database of Systematic Reviews. 2019;8:CD012448.
- Yan F, Pan B, Sun H, Tian J, Li M. Risk factors of coronary artery abnormality in children with kawasaki disease: A systematic review and meta-analysis. Frontiers in Pediatrics. 2019;7:374.
- Yang X, Liu G, Huang Y, Chen S, Du J, Jin H. A meta-analysis of re-treatment for intravenous immunoglobulin-resistant Kawasaki disease. Cardiol Young. 2015;25:1182-90.
- Yang T-J, Lin M-T, Lu C-Y, Chen J-M, Lee P-I, Huang L-M, et al. The prevention of coronary arterial abnormalities in Kawasaki disease: A meta-analysis of the corticosteroid effectiveness. J Microbiol Immunol Infect. 2018;51:321-31.
- Zheng X, Yue P, Liu L, Tang C, Ma F, Zhang Y, et al. Efficacy between low and high dose aspirin for the initial treatment of Kawasaki disease: Current evidence based on a meta-analysis. PloS one. 2019;14:e0217274.
- Lopes E, Street J, Carter D, Merlin T. Involving patients in health technology funding decisions: Stakeholder perspectives on processes used in Australia. Heal. Expect. 2016;19(2):331–44.
|

